Официально
- Комитет по инновациям
- Комитет по образованию, кадровому и профессиональному развитию
- Комитет по стандартизации и обеспечению качества клинических лабораторных исследований
- Комитет по микробиологии
- Комитет по клинической цитологии
- Комитет по молекулярно-биологическим исследованиям
- Комитет по гемостазиологии
- Комитет по гематологии
- Комитет по преаналитике
- Комитет по лабораторной диагностике в неотложной медицине
- Комитет по обращению медицинских изделий для диагностики in vitro
- Комитет по международному сотрудничеству
- Комитет регионального развития лабораторной медицины
- Комитет по информационным технологиям, цифровой медицине и искусственному интеллекту
- Комитет по лабораторной диагностике (среднее медицинское образование)
- Комитет исследований по месту нахождения пациента
- Комитет по иммунологии
- Комитет по референтным интервалам
- Комитет по предиктивной, превентивной и персонализированной медицине
- Комитет по аналитической химии в лабораторной медицине
- Комитет по разработке клинических рекомендаций
- Комитет по обращению образцов биологического материала

Деятельность Ассоциации




Партнеры



Официальная статистика о регистрации медицинских изделий за 2018 г.
Официальная статистика о регистрации медицинских изделий за 2018 г.
В 2018 году было зарегистрировано 1342 медицинских изделия, что на 61 изделие или на 5 % меньше, чем в 2017 году. В 2017 году было зарегистрировано на 62 изделия или на 4,23 % меньше, чем в 2016 году.
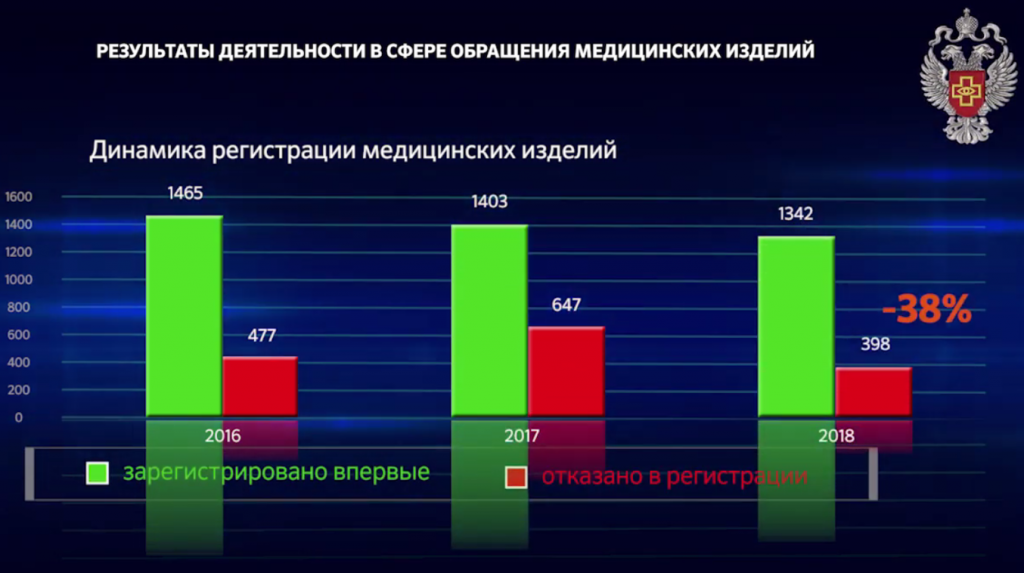
Можно отметить тенденцию к снижению количества зарегистрированных изделий — обратите внимание на линию тренда на диаграмме ниже. Линия тренда в данном случая аппроксимирующая, с прогнозом вперёд на 1 период.
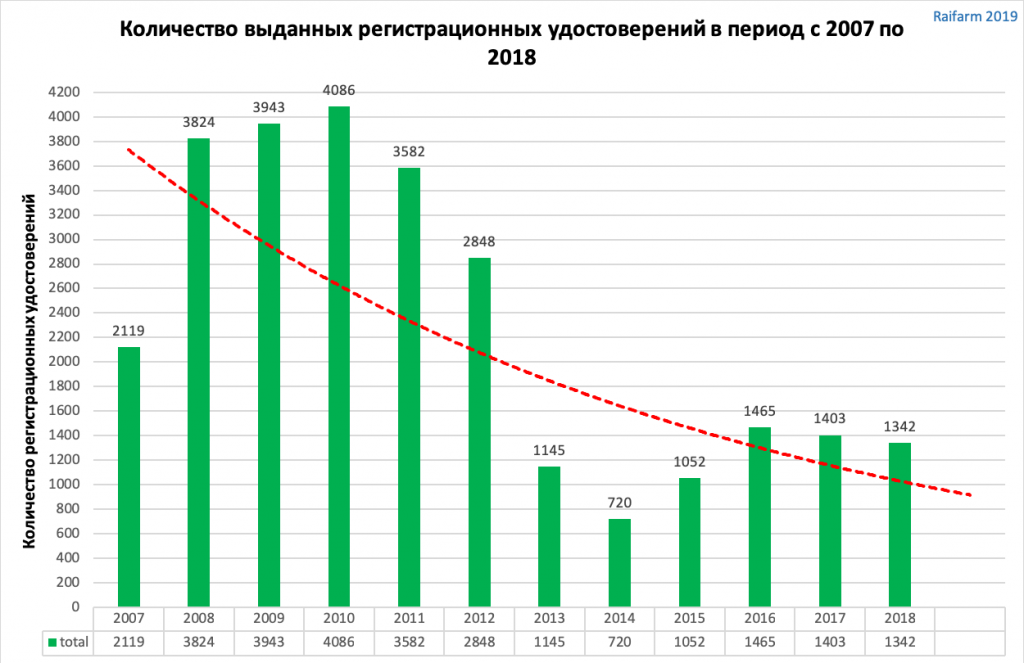
В материале не говорится о причинах снижения количества выданных регистрационных удостоверений, но можно предположить, что одной из основных причин стало всё большее усложнение регуляторных требований. Запросы экспертов о предоставлении материалов и сведений становятся всё сложнее и требуют серьёзных усилий для подготовки всестороннего ответа.
Запросы, в первую очередь, касаются технической, эксплуатационной и нормативной документации, подготовке которой следует уделять самое пристальное внимание. Разночтения в технической документации, предоставляемой производителем, также являются причинами для выдачи запроса. Заявитель должен уделять значительное внимание поиску таких разночтений, причины возникновения которых могут быть самыми разными. Наиболее частые из них — это обычные опечатки или предоставление производителем документа на предыдущую версию изделия.
Также эксперты часто выдвигают требования к маркировке и упаковке изделий, а для изделий со сроком годности требуют предоставления результатов испытаний на стабильность и старение. От регуляторных специалистов требуются всё более серьёзные знания в предметной области и умение ориентироваться в бюрократических хитросплетениях регистрационного законодательства.
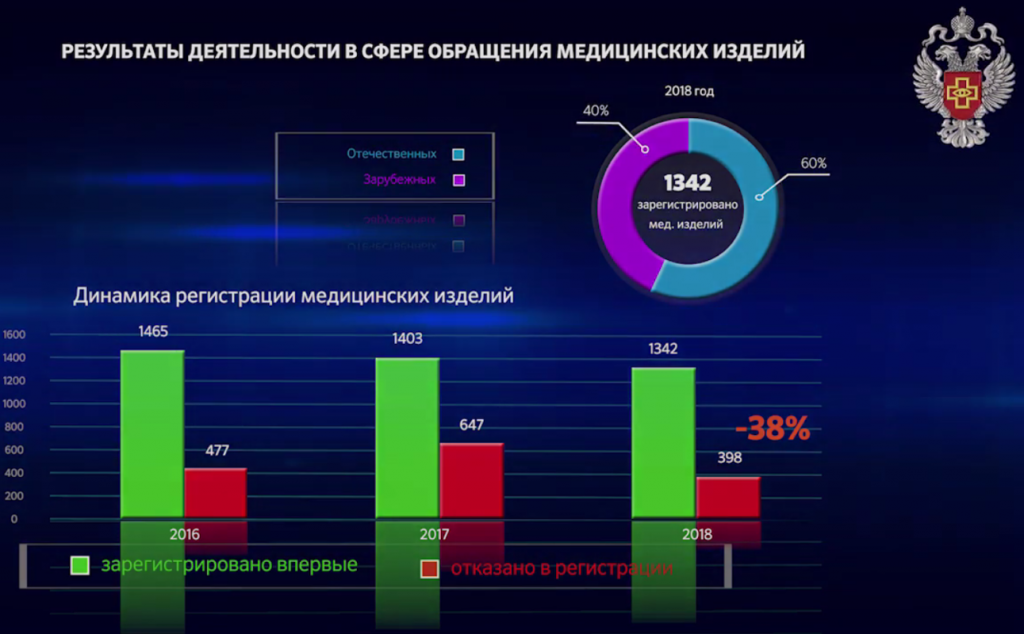
На 60 % отечественных зарегистрированных медицинских изделий приходится 40 % импортных. В абсолютных показателях это 805 регистрационных удостоверений, выданных на отечественную продукцию, и 537 удостоверений на импортную. Информация о количестве зарегистрированных изделий каждого класса риска в этом материале не приводится.
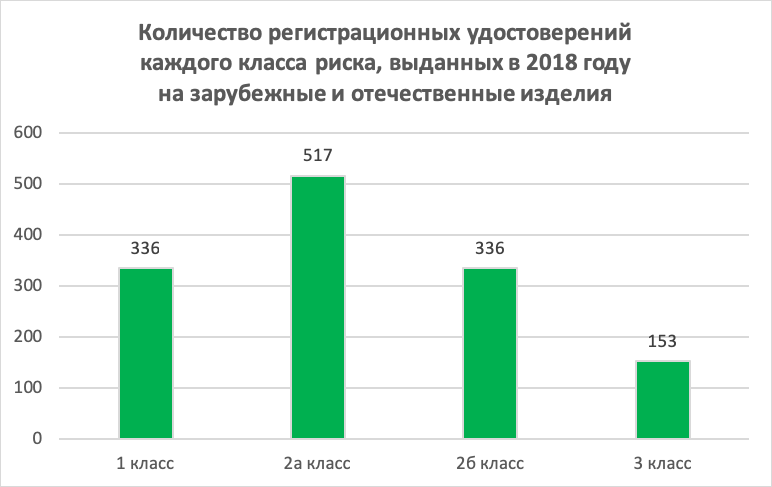
По данным официальной базы Росздравнадзора, за 2018 год на изделия первого класса риска зарубежного и отечественного производства выдано 336 регистрационных удостоверений (25 % от общего числа удостоверений), на изделия 2а класса — 517 регистрационных удостоверений (39 %), на изделия 2б класса — 336 удостоверений (25 %) и на изделия 3 класса — 153 регистрационных удостоверений (11 %).
Также можно отметить снизившееся на 38 % количество отказов в регистрации в 2018 году по сравнению с 2017 годом, но скорее это связано не с эффективностью введённых Росздравнадзором «упрощений», а с тем, что многие регистрационные досье возвращаются заявителям на первом этапе рассмотрения, не доходя до процедуры «экспертизы по существу». Здесь можно вспомнить недавние жалобы заявителей на запросы о предоставлении лицензионных договоров на торговые марки, что в ряде случаев просто невозможно. Сюда же следует отнести запросы, касающиеся частных аспектов устройства и хозяйственной деятельности компаний, что всегда вызывает массу вопросов у зарубежных производителей. В обоих случаях регистрационный процесс заходит в тупик, и комплект документов возвращается заявителю. Такой возврат документов не считается отказом в регистрации.
На диаграмме ниже показано количество выданных регистрационных удостоверений в период с 2007 по 2018 год с детализацией по количеству изделий отечественного и зарубежного производства. Зелёной линией отмечено вступление в силу Постановления Правительства № 1416 «Об утверждении Правил государственной регистрации медицинских изделий». За 2017 год количество регистрационных удостоверений показано суммарно, включая отечественные и импортные. Всего было выдано 1403 регистрационных удостоверения.
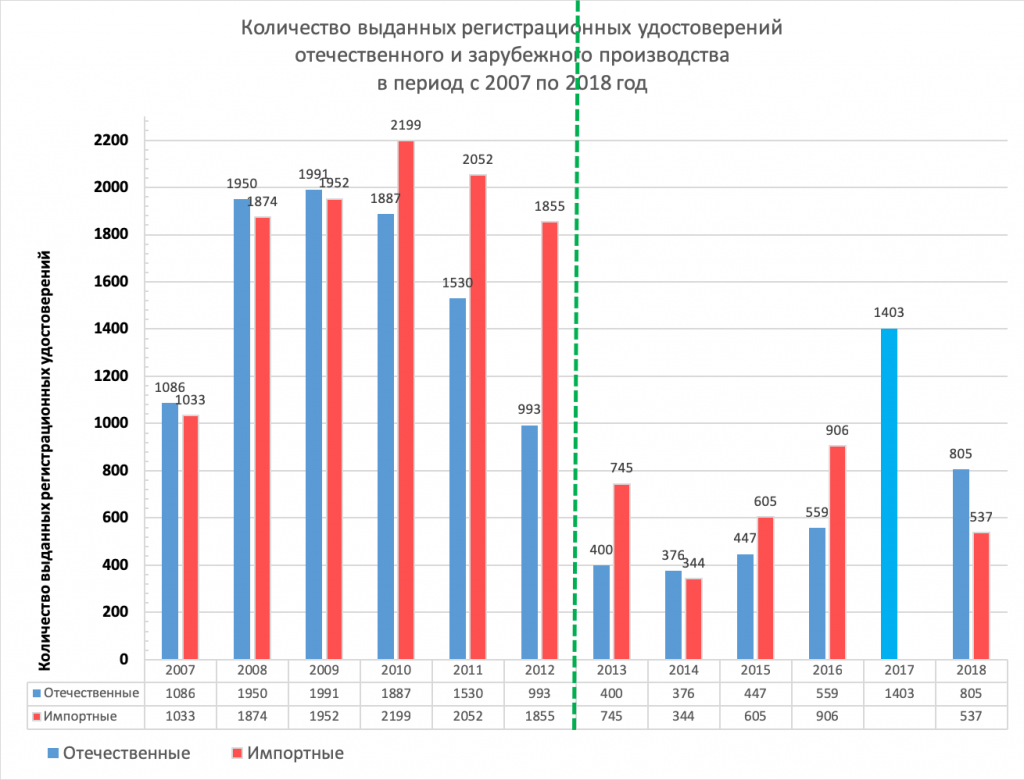
В целом, несмотря на упрощение регистрационной процедуры в отношении изделий 1 класса риска и IVD в 2018 году, регуляторная среда в области регистрации остаётся сложной.
Источник: raifarm.com


